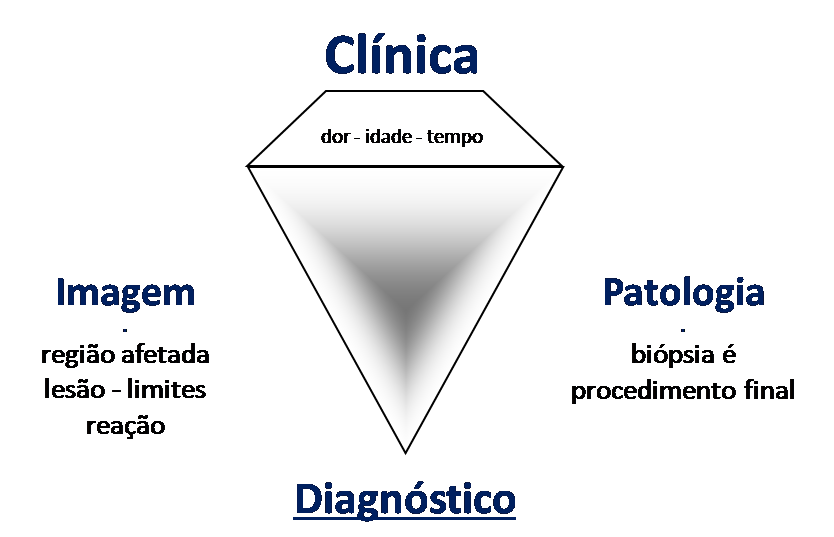
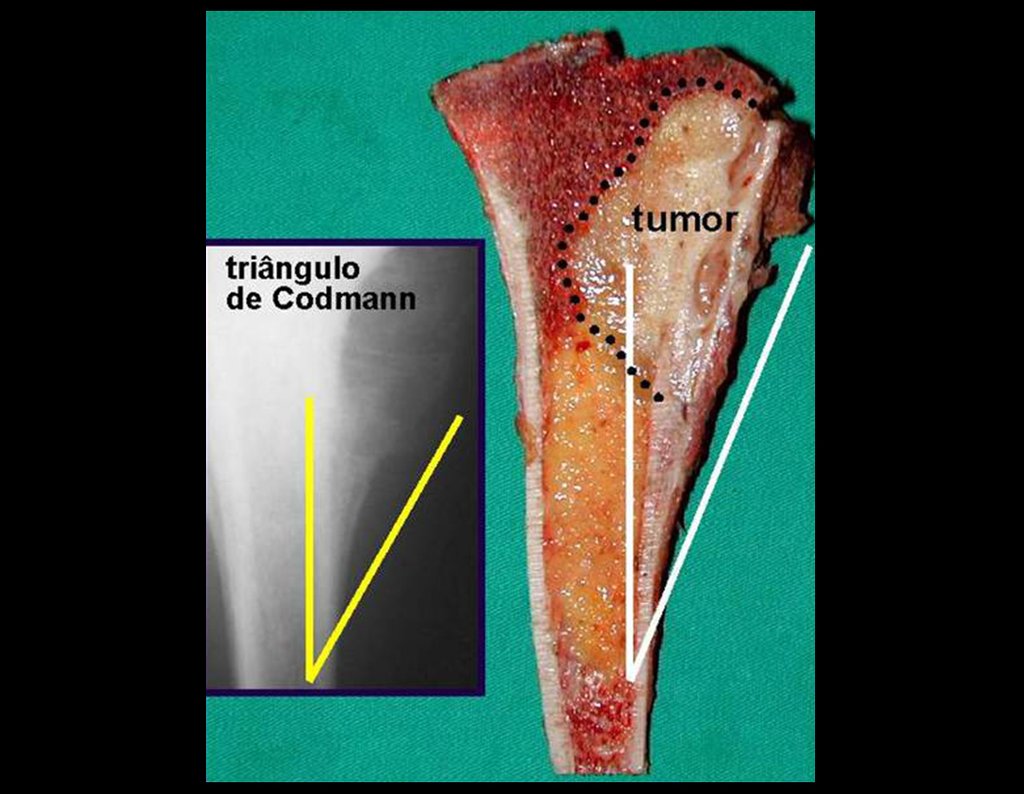
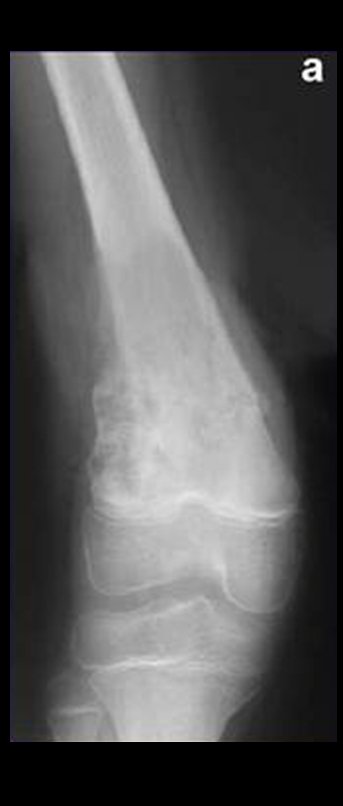
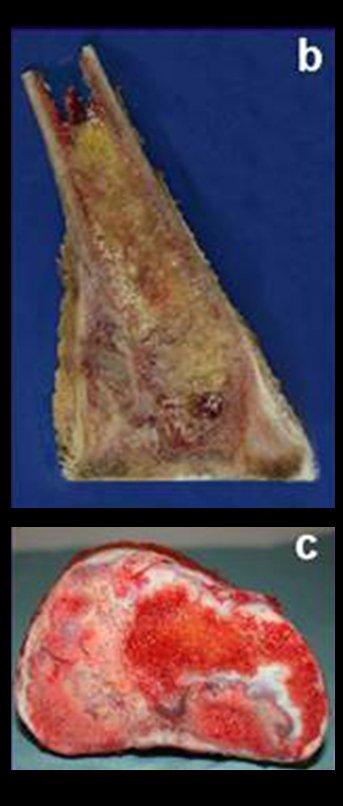
Classificação:
A Organização mundial da saúde (OMS) classifica o sarcoma de tecidos moles de acordo com o subtipo histológico que a neoplasia se assemelha, assim temos o lipossarcoma, o sarcoma sinovial, o rabdomiossarcoma, etc.1
Em alguns casos a histologia é incerta e o aspecto morfológico passa a ser empregado para classificá-los como o sarcoma alveolar ou sarcoma de células claras.
Os sarcomas de tecidos moles mais comuns no adulto são: o indiferenciado, o lipossarcoma, o sarcoma sinovial, o leiomiossarcoma e o tumor maligno de bainha de nervo periférico, que é incluído neste capítulo, apesar de ter origem no ectoderma, pois apresenta comportamento biológico, tratamento e prognóstico semelhantes aos sarcomas de tecidos moles 1,2.
O grau histológico também é usado para classificar os sarcomas de tecidos moles, sendo classicamente divididos em Grau 1, bem diferenciado apresentando baixo grau de malignidade histológica; Grau 2, moderadamente diferenciado e Grau 3, pouco diferenciado com alto grau de malignidade 1.
Quadro clínico:
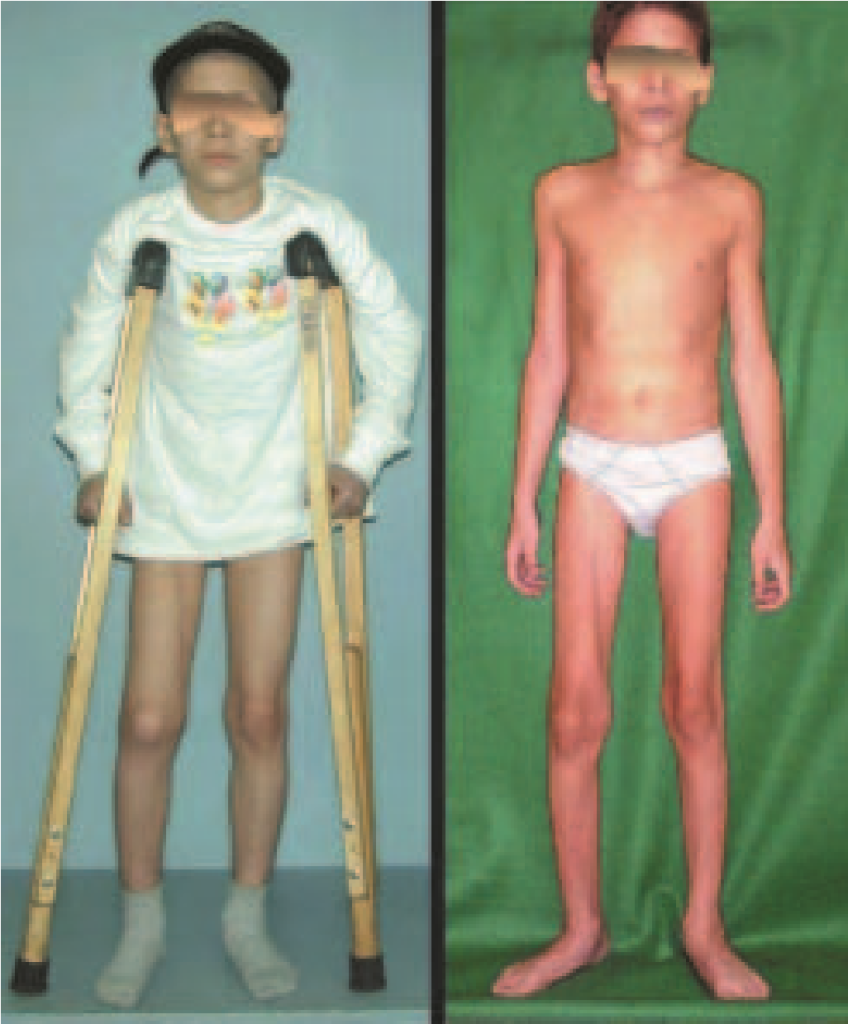
O quadro clínico inicial é de abaulamento tumoral palpável, muitas vezes indolor, com crescimento progressivo podendo chegar a tamanho considerável, principalmente na coxa.
Alguns pacientes podem eventualmente apresentar dor e parestesia por efeito compressivo tumoral. Apresentam-se clinicamente eutróficos, na maioria dos casos, sendo a febre ou o emagrecimento sintomas de exceção.
Os sarcomas de tecidos moles tendem a crescer entre os músculos adjacentes, empurrando e comprimindo as estruturas ao redor, raramente ultrapassam os compartimentos anatômicos. A velocidade de crescimento é variável entre os subtipos histológicos.
Não existem critérios clínicos absolutos para diferenciar os tumores de tecidos moles benignos dos malignos. No entanto, todos os tumores profundos, ou seja, abaixo do plano da fáscia muscular, e os tumores superficiais com mais de 5 cm, têm alta probabilidade de serem malignos 2.
Estadiamento:
No momento do diagnóstico, o sarcoma de tecidos moles raramente apresenta metástase, não ultrapassando 10 por cento dos casos. Isso ocorre mais frequentemente em tumores de grande volume, profundos à fáscia muscular e de alto grau 2.
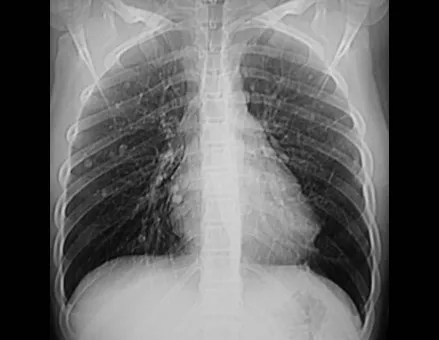
O padrão de disseminação, para a maioria dos sarcomas, é hematogênico e o principal sítio de metástase é o pulmão. Por esse motivo todos os pacientes com sarcoma de tecidos moles devem realizar o estadiamento do tórax. A tomografia do tórax para pesquisa de metástase pulmonar deve ser sempre indicada, principalmente para pacientes com alto risco, como nas lesões superficiais maiores do que 5 cm, tumores profundos e com alto grau de malignidade.
Os linfonodos regionais são sítio de metástases em 2,6 por cento dos casos, porém, em alguns subtipos histológicos estas podem ser mais frequentes e deve ser pesquisado, como no rabdomiossarcoma, sarcoma sinovial, sarcoma epitelioide, sarcoma de células claras e angiossarcoma 2.
A tomografia do abdome e pelve é recomendada, principalmente no estadiamento do sarcoma de tecidos moles de células redondas e lipossarcoma mixóide, pelo alto índice de metástase extrapulmonar para o abdômen e retroperitônio. No caso do angiossarcoma a avaliação do sistema nervoso central, através da tomografia de crânio, é necessária pela propensão de metástase para o encéfalo.
Exames de imagem:
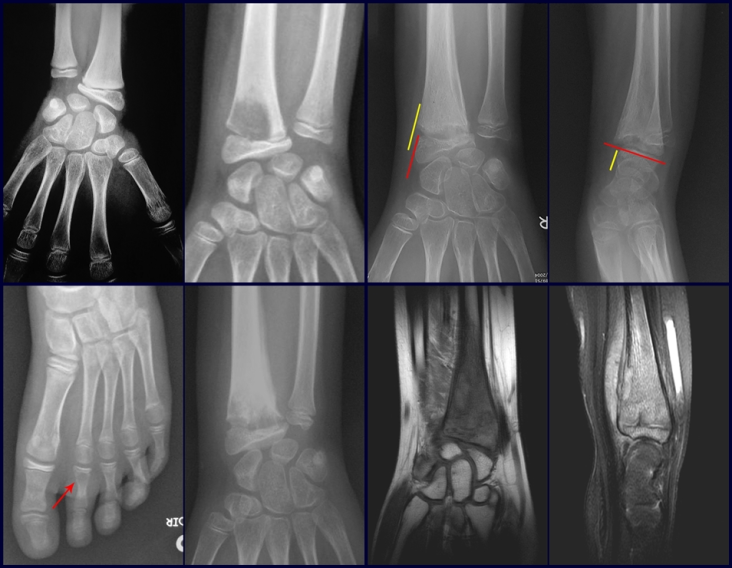
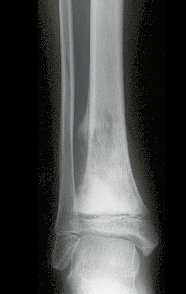
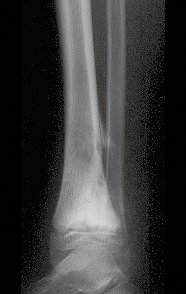
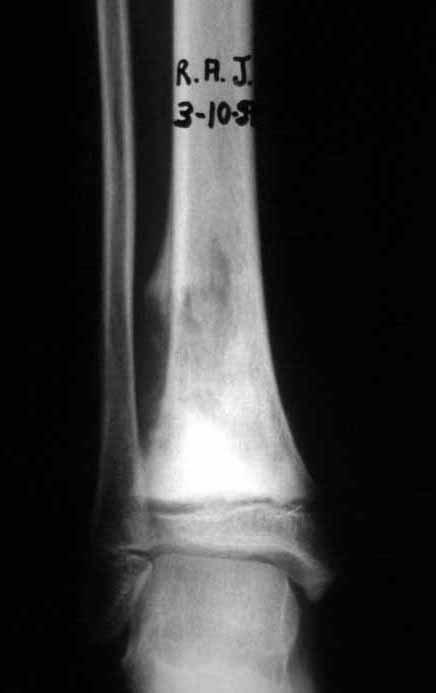
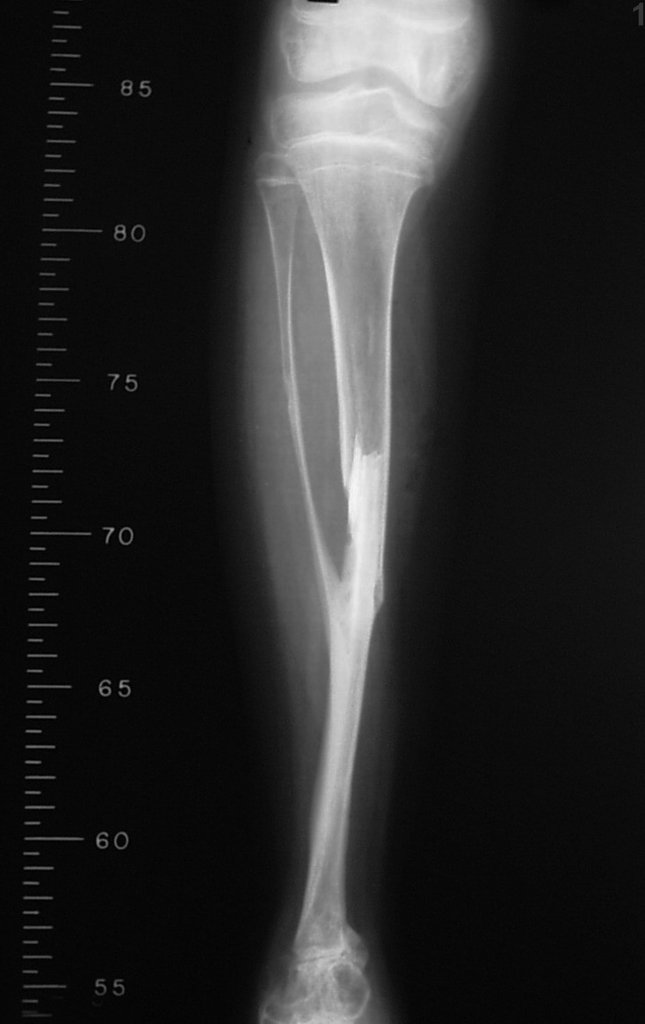
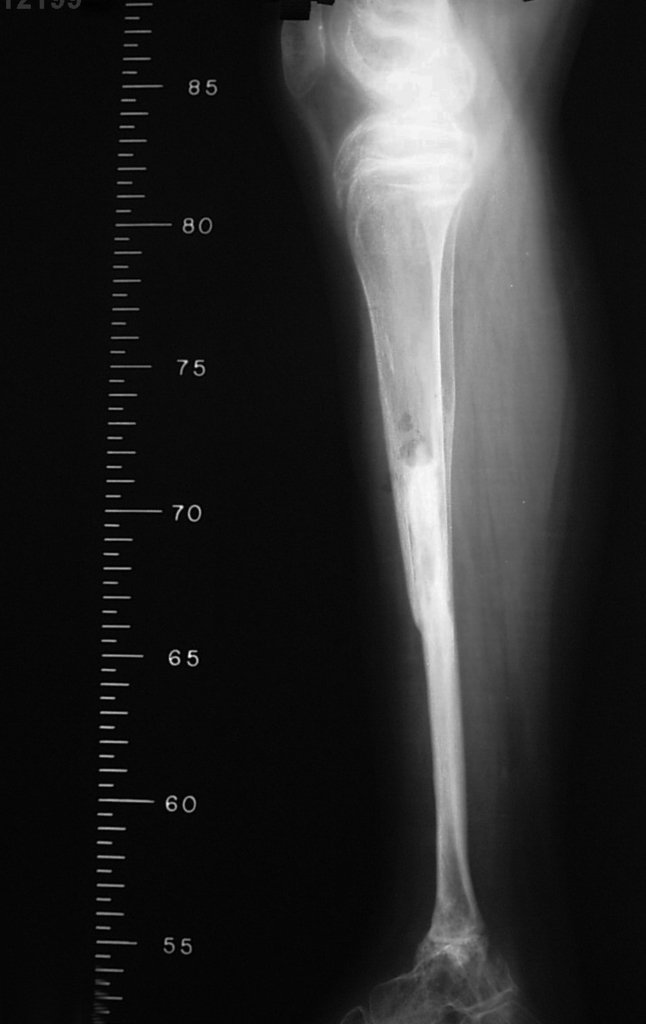
a) Radiografia:
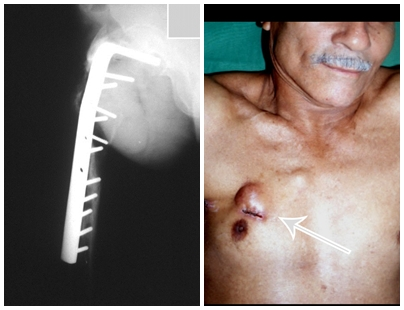
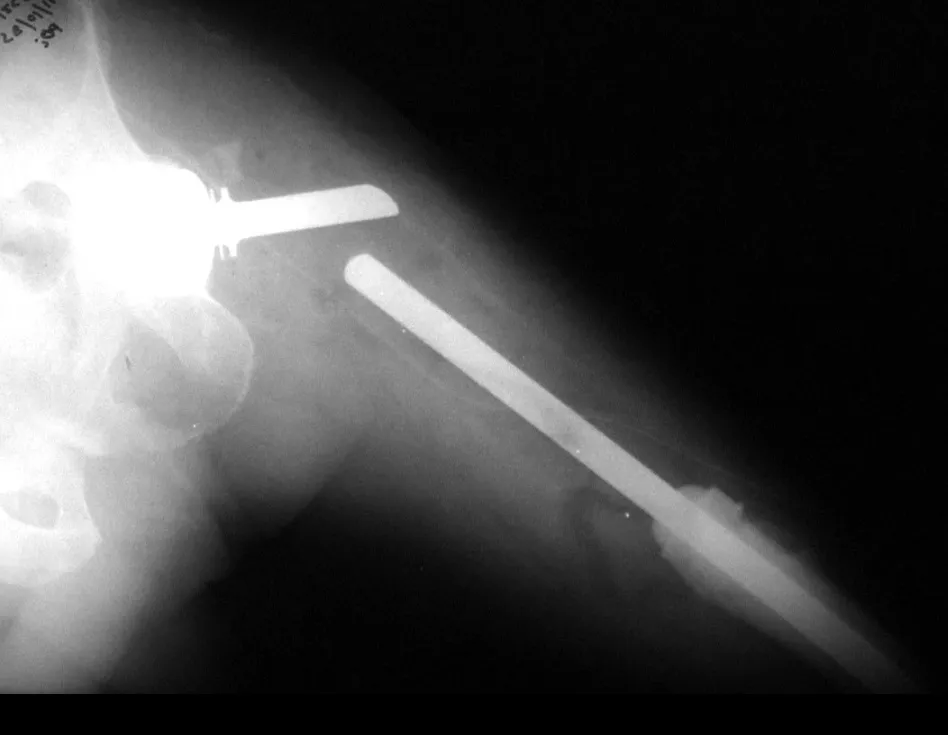
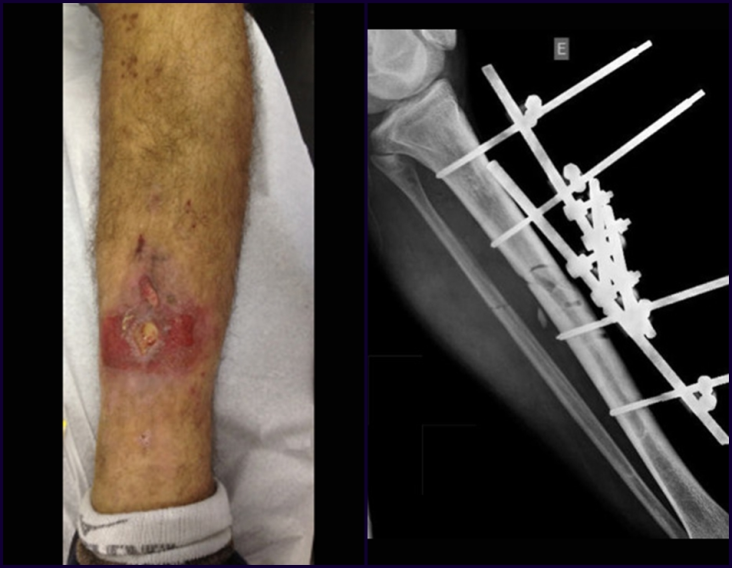
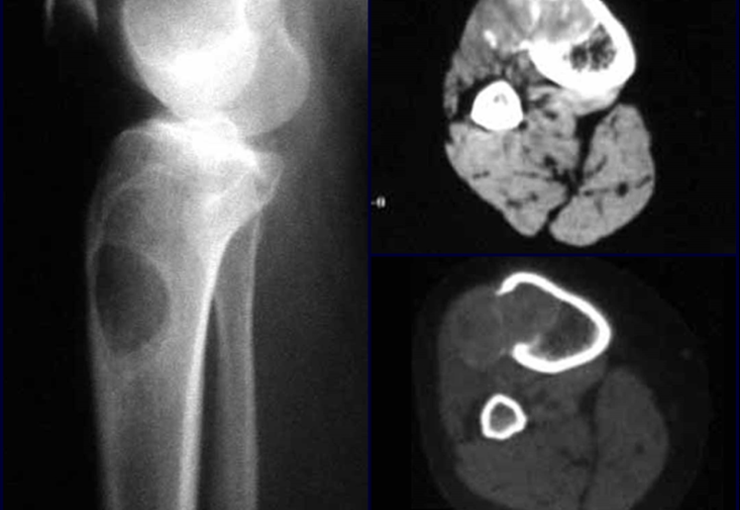
A radiografia é o exame de imagem mais barato e acessível. Pode ser empregada como primeira linha de avaliação dos tumores, para diferenciar um tumor de origem esquelética de um sarcoma de tecidos moles. Além disso, pode evidenciar calcificações no seu interior.
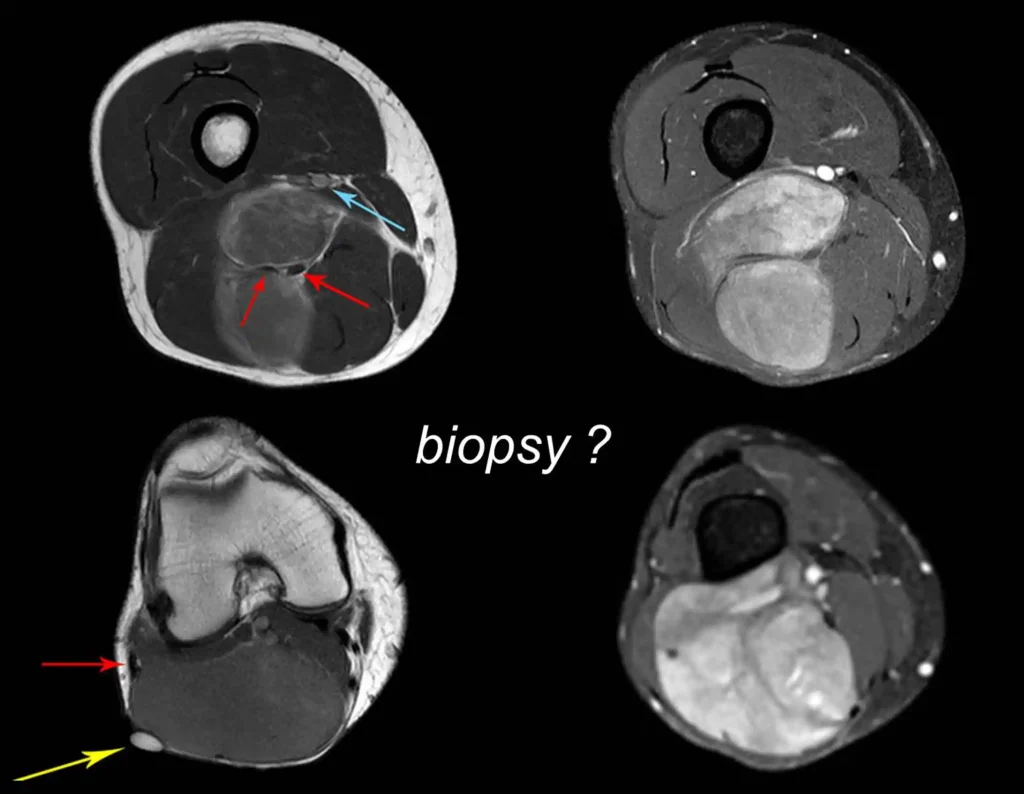
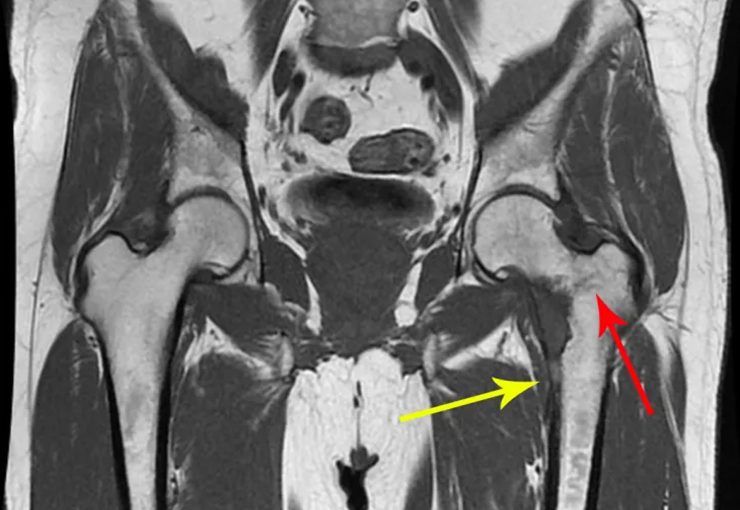
b) Ressonância magnética:
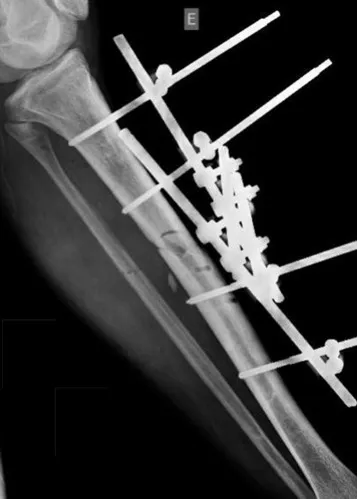
A ressonância magnética ainda é o exame de escolha para avaliar os sarcomas de tecidos moles, quando não há elementos metálicos, como uma prótese ortopédica. Pode detalhar os limites do tumor e a sua relação com as estruturas vizinhas. O uso de contraste pode ainda diferenciar lesões sólidas de lesões preenchidas por liquido, devendo-se solicitar o exame com o emprego de contraste.
c) Tomografia:
A tomografia é o exame de escolha nos tumores do retroperitônio e na pesquisa de metástase pulmonar, pois a ressonância não é adequada devido ao movimento respiratório e ao peristaltismo intestinal. No estudo dos STM de extremidades a ressonância é superior no delineamento da extensão neoplásica 2.
d) Pet-Cet:
A tomografia por emissão de pósitrons com flúor desoxiglicose (FDG-PET/CT) permite, com alta sensibilidade, diferenciar o sarcoma de tecidos moles de alto grau dos tumores benignos de tecidos moles .. Entretanto perde valor na diferenciação entre tumores baixo grau ou graus intermediários 2.
O FDG-PET/CET não deve ser usado de rotina na avaliação inicial de um paciente com tumor em tecidos, porém seu uso é indicado na determinação prognóstica e na resposta ao tratamento quimioterápico 2,3.
O standaruptakevalue (SUV) é uma quantificação da glicose marcada com flúor consumida pelo tumor e demonstra metabolismo tumoral. O sarcoma de tecidos moles com SUV igual ou maior que 6, que após a quimioterapia apresentam redução deste valor menor do que 40 por cento apresentam maior risco de recidiva sistêmica da doença 2.
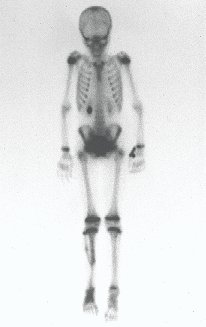
e) Cintilografia:
A cintilografia óssea nem sempre é realizada no estadiamento inicial do sarcoma de tecidos moles, pois metástases ósseas, em adultos, são infrequentes no estágio inicial da doença. A exceção são os tumores de células redondas e o lipossarcoma mixóide, porém o mapeamento do esqueleto pode ser falso negativo e recomenda-se a avaliação através de ressonância magnética 2.
Biópsia:
A biópsia é indicada para o diagnóstico histológico do STM, uma vez que os exames de imagens não apresentam características sugestivas do subtipo histológico, como podemos inferir em algumas neoplasias ósseas, como o osteossarcoma.
A biópsia nem sempre é necessária para o tratamento, pois o tratamento dos STM ainda hoje é prioritariamente cirúrgico e, em alguns casos, a biópsia pode ser substituída pela ressecção excisional ou também chamada de biópsia excisional.
Tumores superficiais, acima da fáscia muscular, menores do que 5 cm, apresentam baixa probabilidade de serem malignos. Nestes casos podem ser ressecados sem diagnóstico histológico se forem passiveis da realização de cirurgia oncológica (ressecção ampla com margem oncológica, sem comprometer estruturas nobres ao redor), pois este seria o tratamento correto na eventualidade de estarmos tratando de um sarcoma de tecidos moles de alto grau.
A biópsia deve ser realizada pelo cirurgião que fará o tratamento definitivo ou ser orientada por ele. O trajeto da biopsia deve estar em linha com a incisão que será usada na ressecção e todo este trajeto de biópsia deve ser removido em bloco, juntamente com o tumor.
A biópsia incisional, realizada através de uma incisão cirúrgica, expondo parte do tumor foi a mais utilizada para o diagnóstico do sarcoma de tecidos moles. Atualmente as biópsias percutâneas ganharam espaço com o desenvolvimento de agulhas apropriadas, como a trucut®, e aos métodos de imagem como o ultrassom e a tomografia para guiá-las.
Patologia:
O patologista deve sempre estar presente, para realizar o exame de congelação, visando confirmar e garantir que o material coletado é representativo da lesão, evitando-se a necessidade de repetição do procedimento. O resultado histológico definitivo deverá aguardar a histologia em parafina e eventualmente a imuno-histoquímica.
A biópsia percutânea com agulha, feita com estes cuidados, geralmente permite diferenciar tumores malignos de benignos e os patologistas experientes conseguem determinar corretamente o grau histológico dos tumores em respectivamente 97,6 e 86,3 por cento, além desta técnica provocar menor disseminação local da lesão, durante o procedimento 3.
Sarcoma de tecidos moles – Tratamento:
O tratamento dos tumores de tecidos moles é geralmente cirúrgico, entretanto, como na maioria das neoplasias o acompanhamento do paciente oncológico deve ser sempre multidisciplinar.
Desde o diagnóstico ao estadiamento e tratamento uma equipe de vários profissionais interage na condução do caso, como o ortopedista que realizará a cirurgia oncológica, o patologista, o radiologista, o oncologista clínico, o radioterapeuta, o psicólogo, o assistente social, etc.
O objetivo do tratamento é preservar a vida do paciente, evitando-se a recidiva local, maximizando a função do membro afetado e minimizando a morbidade do tratamento.
Quimioterapia:
Os Sarcomas de tecidos moles, da população pediátrica, respondem a quimioterapia sistêmica por apresentar maior resposta às drogas, propiciando melhora na sobrevida, pois a criança consegue suportar as doses de quimioterápicos necessárias para o controle da enfermidade, diferentemente dos adultos.
Nas crianças, os sarcomas de tecidos moles mais comuns são o rabdomiossarcoma, a forma extra óssea do osteossarcoma e a forma extra óssea do sarcoma de Ewing. Todos estes com protocolos quimioterápicos neoadjuvante e adjuvante.
Nos raros casos de ocorrência dessas neoplasias em adultos opta-se pelo protocolo quimioterápico pediátrico, nas doses suportadas para o adulto e suas eventuais comorbidades.
Nos sarcomas de tecidos moles do adulto, existe uma grande polêmica quanto ao uso da quimioterapia. A meta-analise publicada em 1997 pelo Sarcoma Meta-analysiscollaboration evidenciou que o uso de doxorubicina nestes pacientes aumentou o tempo livre de recidiva local e metástase a distância, porém não houve benefício estatisticamente significativo na sobrevida global dos pacientes 3.
Uma nova meta-análise atualizada foi publicada em 2008 demonstrando que o uso da doxorubicina associada a ifosfamida promoveu melhoria na sobrevida dos pacientes 3. No entanto, a quimioterapia é extremamente tóxica, principalmente na população adulta em que a presença de comorbidades clínicas pode tornar o tratamento efetivo inviável. A recomendação atual é individualizar cada caso, lembrando que o tratamento sistêmico não corrige uma ressecção cirúrgica inadequada.
De forma geral, os STM do adulto, são maus respondedores a quimioterapia. O tratamento, portanto, recai sobre a ressecção cirúrgica.
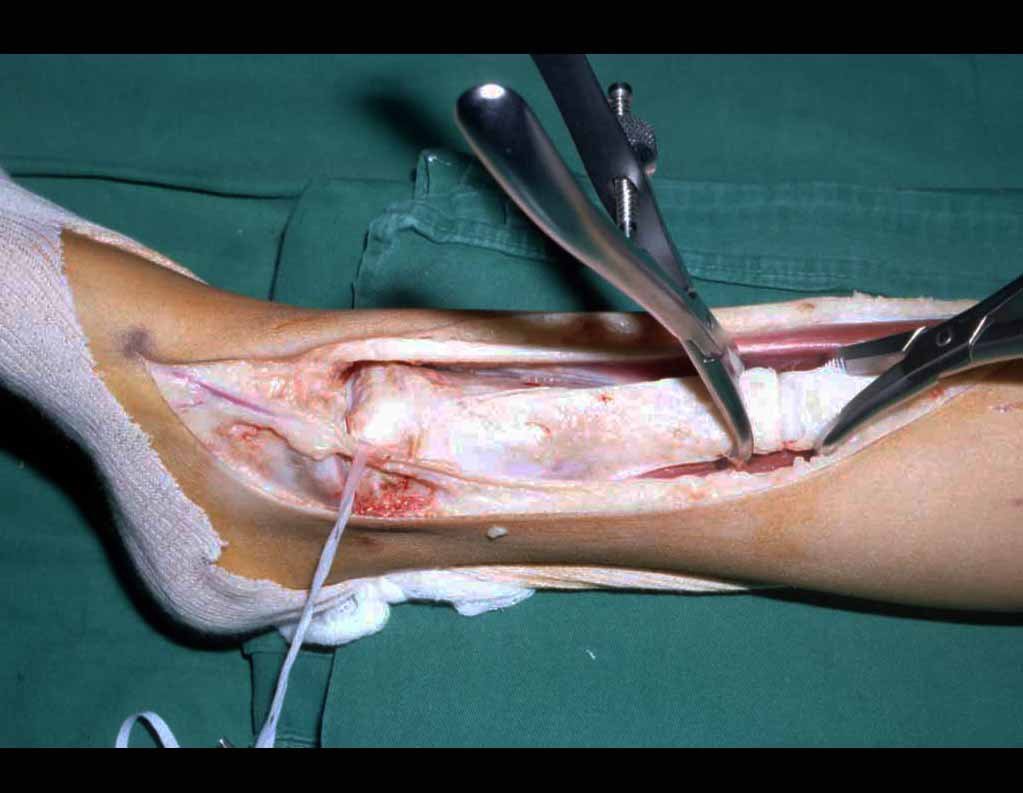
Cirurgia oncológica:
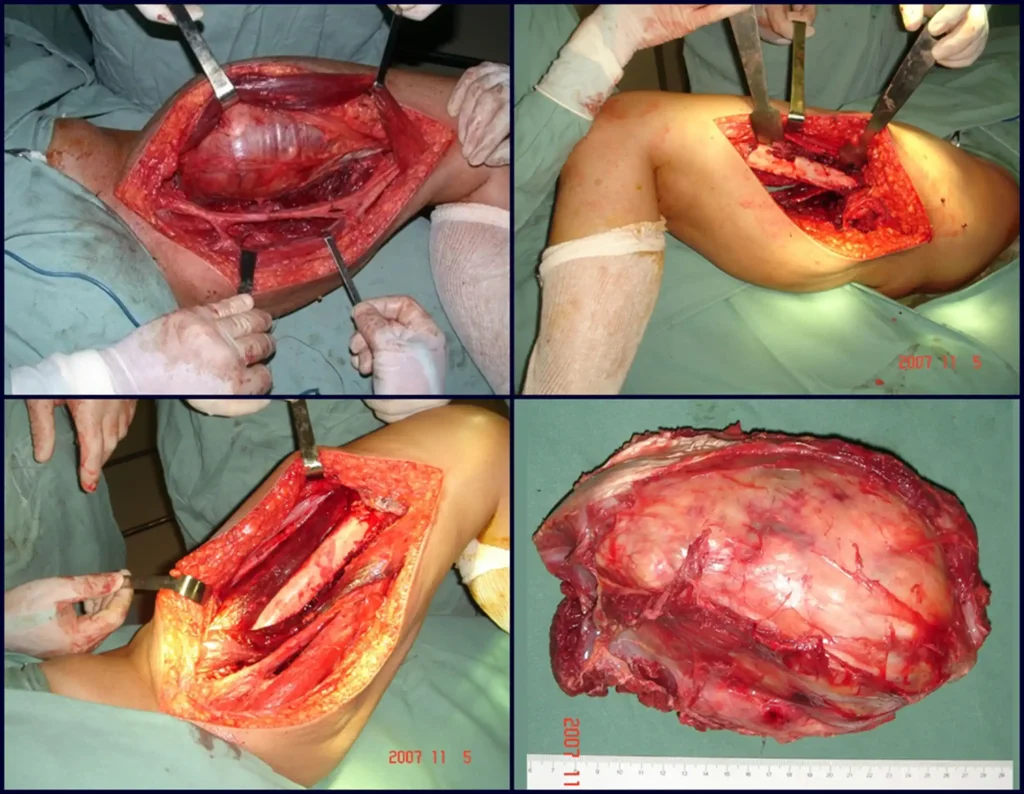
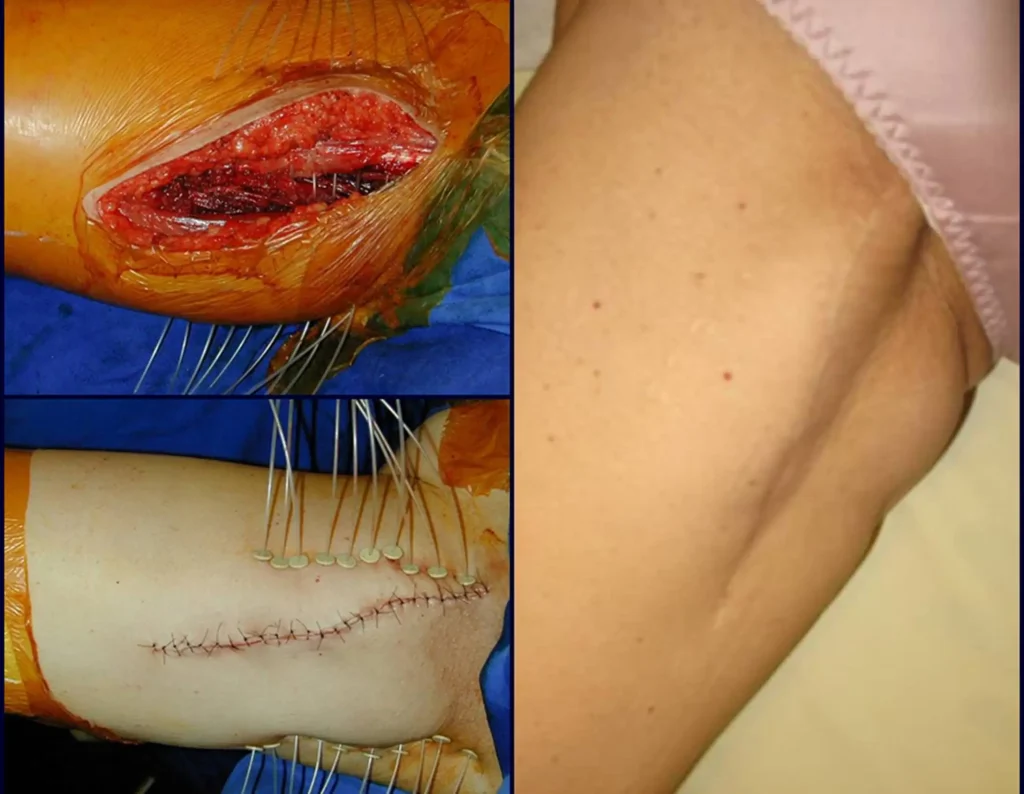
A cirurgia de ressecção do sarcoma de tecidos moles deve ser realizada com margens amplas, de forma que todo o tumor seja retirado em bloco e revestido por tecido saudável, visando garantir que não existam células neoplásicas residuais após a ressecção.
Os sarcomas de tecidos moles apresentam uma pseudocapsula ao redor. Esta estrutura é representada por um processo inflamatório produzido pela agressão tumoral e nem sempre é barreira suficiente para as células neoplásicas, que permeiam os tecidos ao seu redor. Pode-se indicar radioterapia adjuvante visando atuar nas margens quando estas precisarem ser exíguas, devido a necessidade de preservação de estruturas nobres, como vasos e nervos.
A ressecção tumoral através da pseudocapsula pode deixar tecido neoplásico microscópico no paciente podendo ser fator de risco para recidiva local e pior prognóstico.
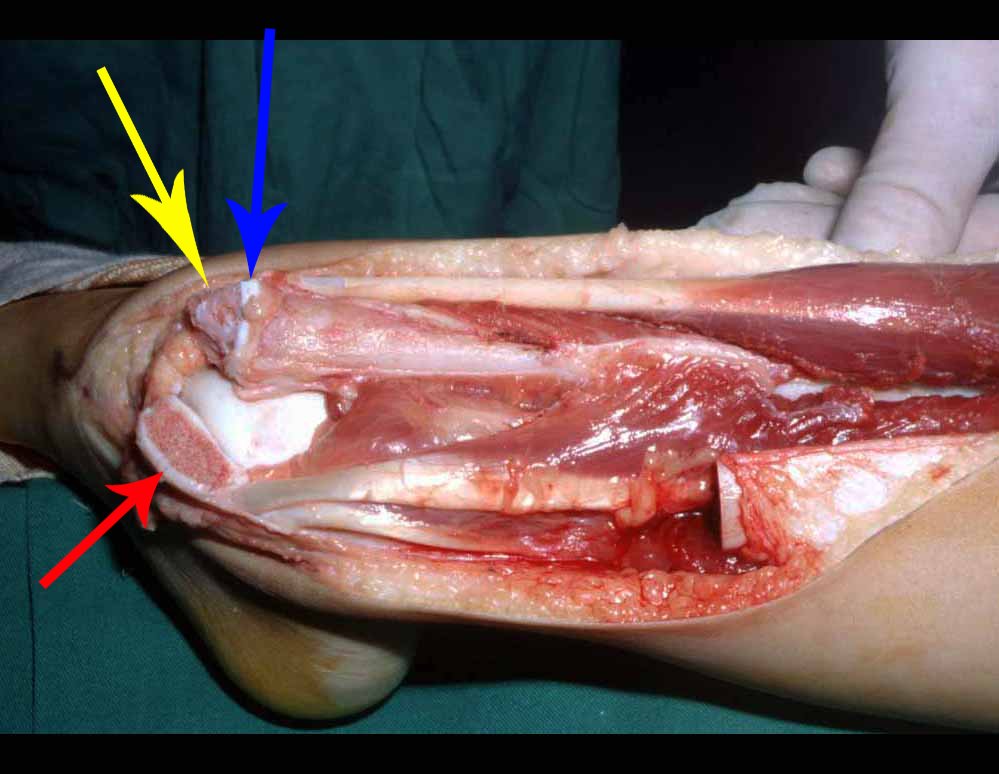
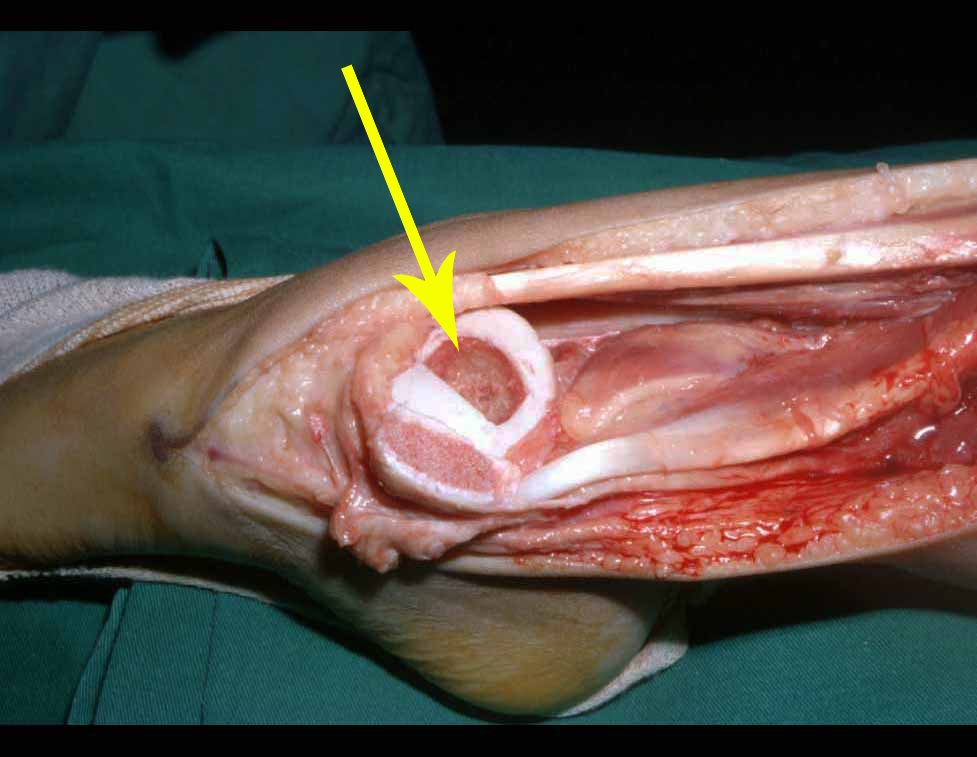
Os sarcomas de tecidos moles tendem a crescer expandindo-se e empurrando os tecidos ao redor, mas raramente infiltrando-o. Dessa forma, é incomum a invasão óssea ou dos tecidos musculares adjacentes.
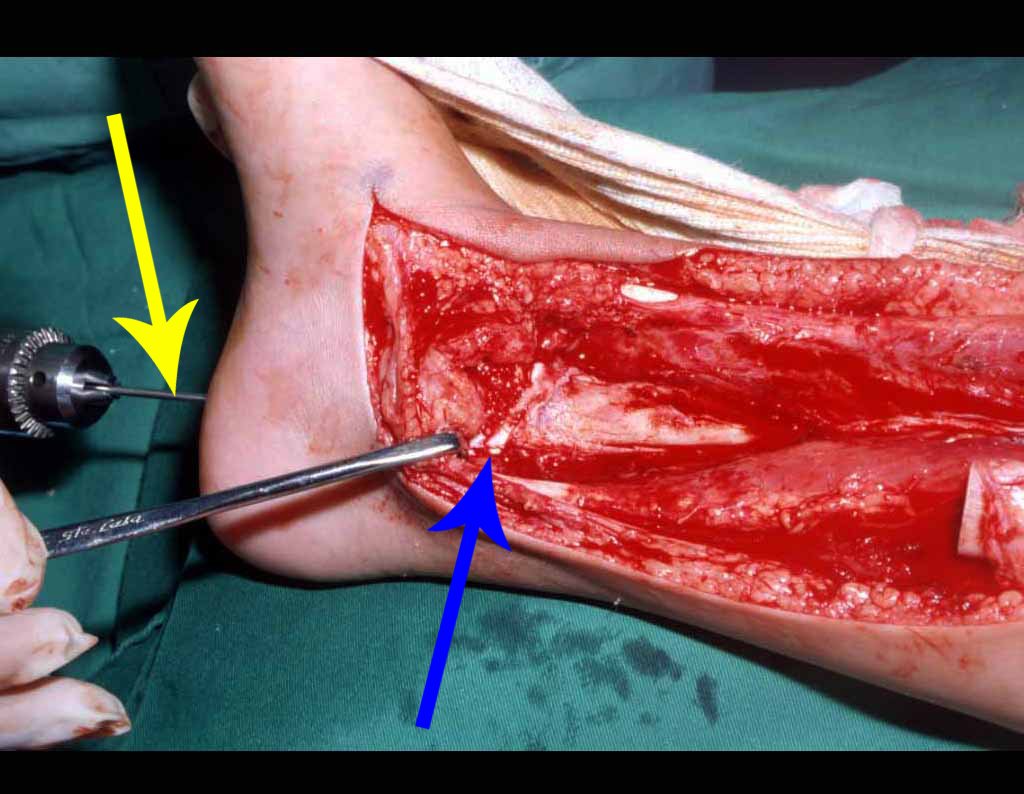
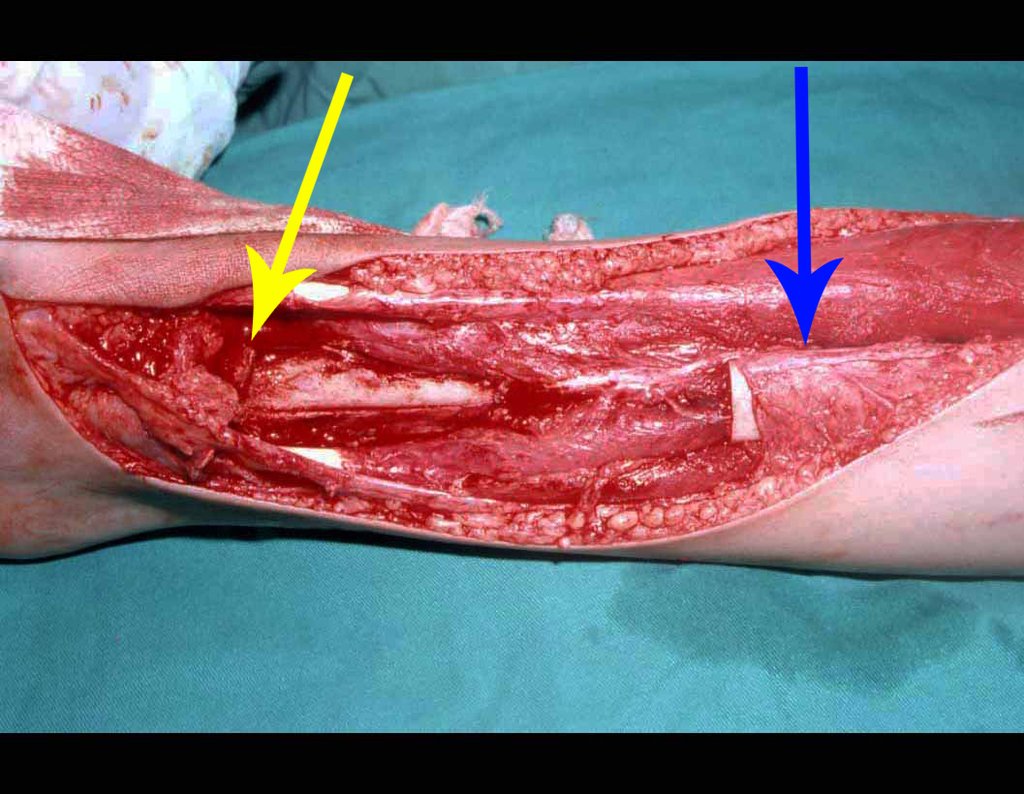
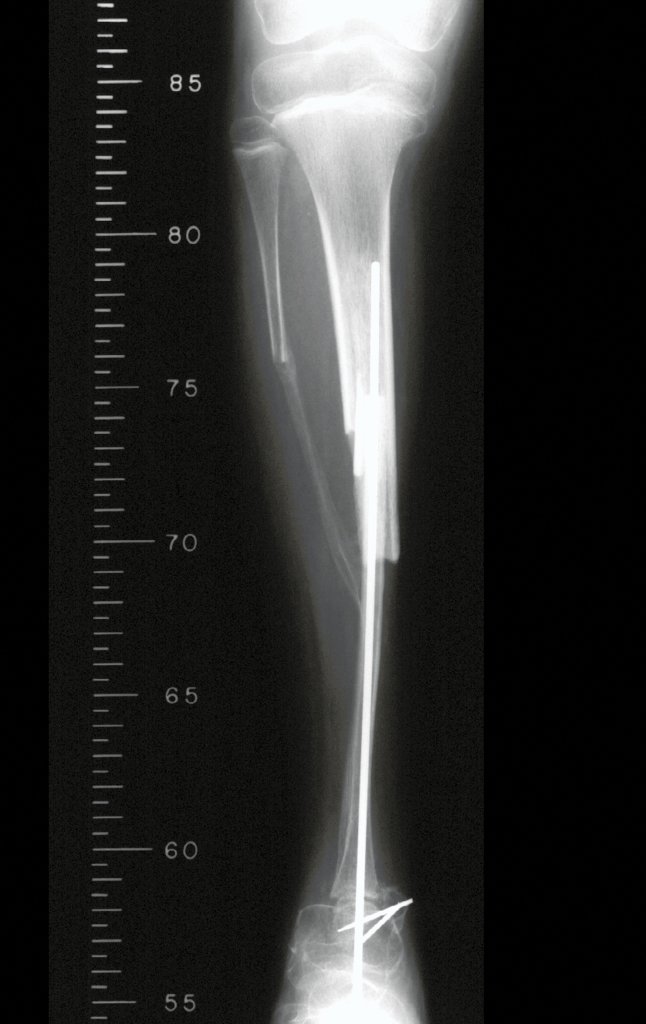
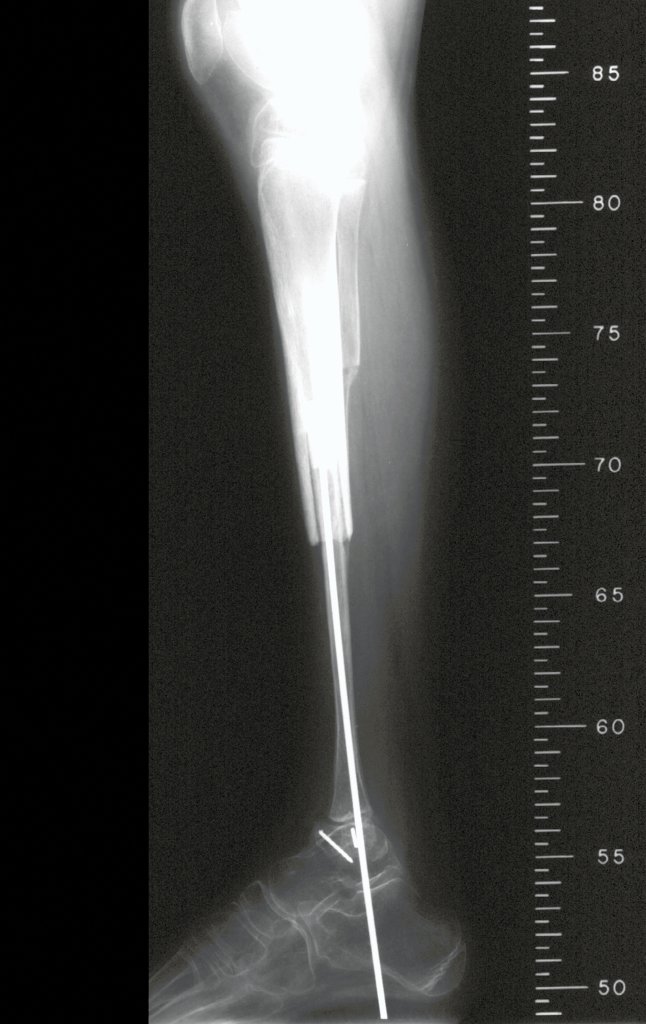
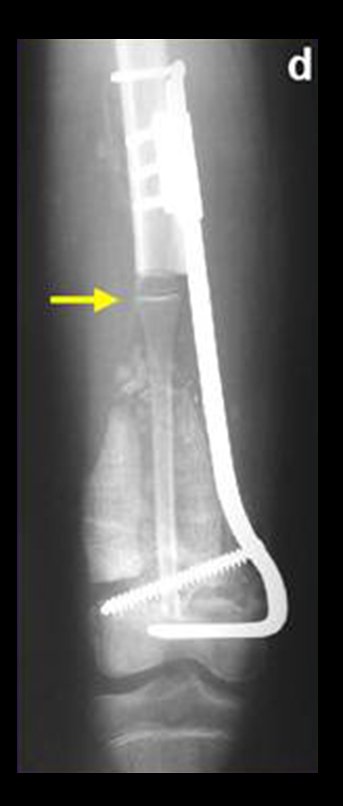
Na maioria das vezes em que o tumor se aproxima do osso é possível dissecá-lo retirando-se o periósteo que envolve o osso em questão, juntamente com o tumor. Esta desperiostização associada a radioterapia, que geralmente é usada como adjuvância, aumentam o risco de fratura, especialmente no fêmur 4.
Recorrência:
A espessura das margens amplas ao redor do tumor é questionável, sendo recomendado 1 cm, mas isso dificilmente acontece de maneira homogênea em toda sua circunferência.
Para preservar tecidos nobres, como grandes nervos ou vasos, eventualmente o cirurgião reduz essa margem para evitar a ressecção de tal estrutura, que pode colocar em risco tanto o paciente quanto o próprio membro em que se busca preservar a melhor função.
Por outro lado, os planos dos tecidos anatômicos representam diferentes barreiras ao tumor, como a fáscia muscular em que 1 a 2 milímetros de margens pode ser adequado, para uma ressecção segura.
Outros tecidos como a gordura ou o ventre muscular necessitam de margens mais amplas.
Grandes nervos podem ser preservados dissecando-se e retirando-se a bainha nervosa externa como margem, uma vez que os sarcomas de tecidos moles não costumam infiltrar os nervos. Quando o tumor circunda o nervo, há maior dificuldade técnica e este nervo pode necessitar ser seccionado e reconstruído com sutura microcirúrgica.
Enxertos nervosos para reconstrução raramente são úteis nos membros inferiores de adultos, especialmente em sitio que precisará ser irradiado. As crianças, entretanto, podem apresentar resultados melhores.
A cirurgia ablativa é geralmente evitada, pois mesmo uma função limitada do membro inferior pode ser viável, mesmo nos casos que necessitem de ressecção completa do nervo ciático.
Radioterapia:
O uso da radioterapia adjuvante promove a destruição das células tumorais ao redor da lesão principal. Quando associada a ressecção cirúrgica preservadora do membro promove aumento do controle local minimizando a recidiva para 10 a 15% 4. No entanto a associação dessa modalidade terapêutica não aumenta a sobrevida global.
A radioterapia é indicada para quase todos os casos de sarcoma de tecidos moles.
A ressecção cirúrgica exclusiva pode ser suficiente para os casos de tumores superficiais de baixo grau ou em tumores de pequeno volume, totalmente intramusculares, desde que as margens amplas estejam garantidas na cirurgia oncológica realizada.
Com a melhora no controle local, a radioterapia como adjuvância nos sarcomas de tecidos moles reduziu o índice de amputação de extremidades de 50% na década de 1970 para 1% atualmente, sem prejuízo da sobrevida 5.
A indicação de amputação na presença de STM pode ser necessária em tumores excessivamente extensos, de forma que o membro residual não tenha função.
Um exemplo é a necessidade de ressecar-se um tronco nervoso principal, como o plexo braquial com impossibilidade de obter-se margens amplas. Neste caso, a perda da sensibilidade resulta em um membro remanescente inviável.
O comprometimento de grandes vasos pelo tumor, já foi uma indicação de amputação no passado, porém com a técnica de reconstrução vascular tornou-se possível ressecar o tumor em bloco com os vasos e reconstruí-los com enxerto vascular, permitindo um membro viável.
Margens cirúrgicas:
A principal variável no controle local da doença são as margens cirúrgicas da ressecção tumoral 5.
A presença de margens coincidentes com o tumor aumenta o risco de recidiva local e a recidiva aumenta o risco de metástase a distância o que pode levar a menor sobrevida.
A presença de margens comprometidas, no entanto, não representa certeza de recidiva local, uma vez que apenas 30 por cento dos casos submetidos a ressecção incompleta, submetidos a radioterapia adjuvante sofreram recidiva.
As margens amplas, por outro lado, também não são garantia de controle local, uma vez que, mesmo quando associada à radioterapia, a recidiva nessa situação gira em torno de 5 a 10 por cento.
A presença margens positivas na ressecção podem requerer nova abordagem do leito cirúrgico, buscando ampliação das margens previamente obtidas.
Esta nova abordagem dependerá da análise sobre qual estrutura anatômica necessitará ser ressecada para essa ampliação.
Em centros de referência em cirurgia oncológica, a presença de margens comprometidas normalmente está relacionada a eventual tumor residual em grandes feixes nervosos que necessitariam de amputação para sua ressecção. Se for este o caso, pode-se utilizar dose maior de radioterapia (66-68 Gy) ou optar-se pela amputação, como último caso.
Tumores de tecidos moles benignos:
Os tumores benignos de tecidos moles são cem vezes mais comuns do que os tumores malignos. Dentre eles o lipoma subcutâneo está entre os mais diagnosticados na prática clínica.
Estas lesões não causam dor e são diagnosticadas quando são superficiais e fazem saliência na pele ou quando são profundas e atingem grande volume. A exceção é o schwannoma que surge de um nervo periférico e pode apresentar dor, parestesia e menos frequentemente alteração motora.
Apesar de benignos, com o crescimento desses tumores pode ocorrer compressão de estruturas adjacentes e só então aparecerem os sintomas.
O tratamento da maioria dos tumores benignos de tecidos moles é dependente dos sintomas que eventualmente produzam. Como a maioria deles são assintomáticos, a ressecção cirúrgica é indicada quando estão aumentando de tamanho, causando desconforto ou alteração estética.
Em tumores superficiais, de pequeno tamanho, assintomáticos e sem sinais sugestivos de malignidades nos exames de imagem, pode-se optar por observar a evolução clínica.
O tumor desmoide, apesar de benigno, é uma neoplasia de tecidos moles localmente agressiva, que produz sintomas pela agressão aos tecidos vizinhos.
Ao contrário da maioria das neoplasias de tecidos moles benignas, a ressecção do desmoide deve ser indicada com margens amplas, cirurgia oncológica semelhante ao tratamento para os tumores malignos.
O tumor desmoide é altamente recidivante, mesmo após ressecção adequada. Em alguns casos o paciente pode necessitar de amputação do membro devido às inúmeras recidivas, ou quando apresentar dor ou disfunção intratável e uma nova ressecção tornar-se impossível.
Discussão:
- Uma consideração é a realização de biópsia prévia ou biópsia excisional (ressecção biópsia) nos casos de sarcomas de tecidos moles pequenos, superficiais, ou em locais em que é possível a cirurgia oncológica, com amplas margens em toda a circunferência do tumor?
- Outra consideração é quanto aos sarcomas de tecidos moles do adulto, em que a quimioterapia neoadjuvante não melhora localmente e nem interfere na sobrevida, há uma controvérsia quanto a realização de radioterapia neoadjuvante:
- A) Radioterapia + cirurgia + radioterapia ou
- B) Cirurgia + radioterapia?
O Quadro 2 abaixo sintetiza parâmetros que devemos considerar.